Wie wirkt eine Impfung
Impfen soll das körpereigene Abwehrsystem des Geimpften zu einer spezifischen Immunantwort gegen bestimmte Krankheitserreger oder ihre krankmachenden Faktoren verhelfen. Im Rahmen der Impfung soll das Immunsystem die in der Vakzine enthaltenen Antigene (abgeschwächte oder abgetötete Krankheitserreger oder Bestandteile von ihnen) erkennen und auf sie durch die Bildung von Antikörpern und die Aktvierung von Abwehrmechanismen durch Zellen zur Beseitigung dieser Antigene reagieren. Darüber hinaus wird durch die Schaffung eines immunologischen Gedächtnisses (durch „Gedächtniszellen“) garantiert, dass in der Zukunft bei Eindringen der echten Krankheitserreger die körpereigene Abwehrkräfte entweder so stark sind, dass eine Infektion von Beginn an abgeblockt oder die Erkrankung verhindert wird.
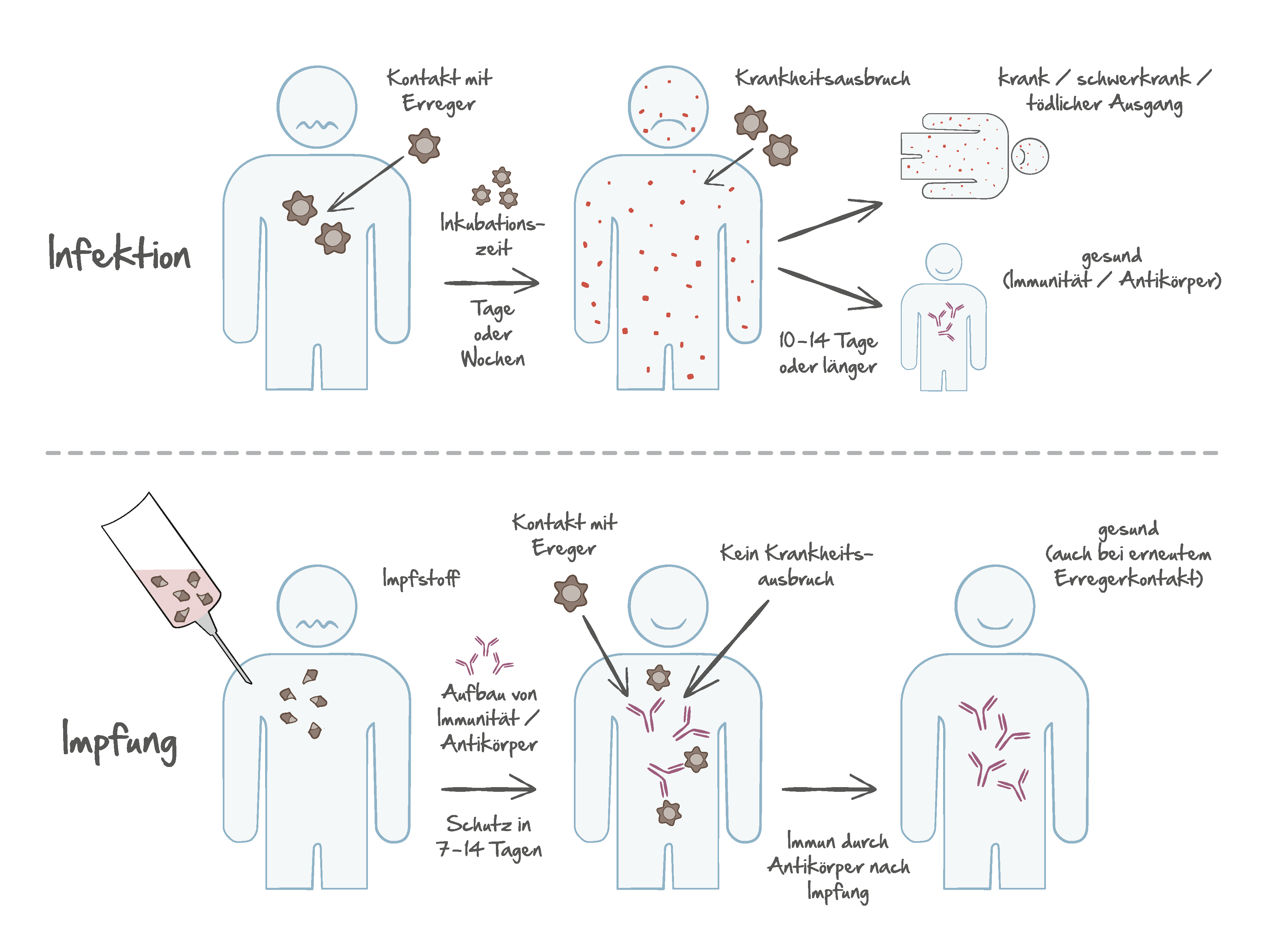
Die Abläufe nach einer Impfung sind sehr ähnlich wie bei einer „echten“ Infektion durch die natürlich vorkommenden Krankheitserreger. Die durch die Impfung hervorgerufene Immunreaktion entsteht in mehreren Phasen:
Antigenerkennungsphase: Während dieses Zeitabschnittes erkennen bestimmte weiße Blutkörperchen (Lymphozyten) das Antigen (immunologisch wirksames Merkmal) aus der Vakzine, schlagen Alarm und aktivieren jene Abwehrzellen, welche für die spezifische Abwehr notwendig sind. Aktivierungsphase: B- und T-Lymphozyten, die mit dem Antigen in Kontakt gekommen sind, vermehren sich durch Klonierung (= Vervielfältigung einer bestimmten Zelle). Es entstehen völlig idente Abwehrzellen, die ebenfalls jenen Rezeptor an der Oberfläche tragen, mit welchem sie an das Antigen andocken können.
Aus den Antigen-spezifischen B- und T-Lymphozyten gehen Effektorzellen hervor, welche bei einem Kontakt mit dem natürlichen Krankheitserreger, gegen den der Impfstoff schützen soll, diesen sofort eliminieren können. Nach der Impfung beseitigen sie die Antigene der Vakzine als wären diese die natürlichen Krankheitserreger.
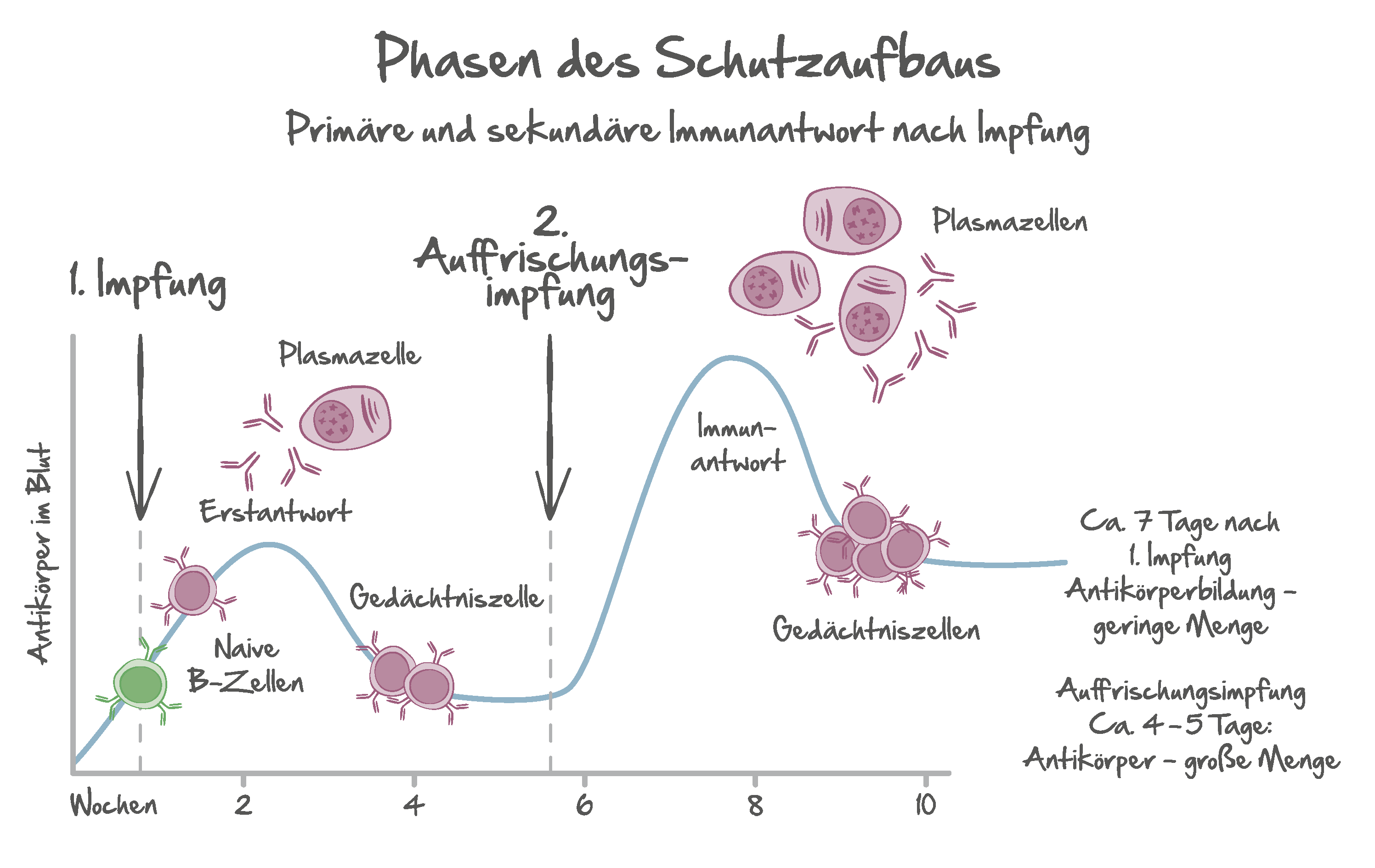
Die Effektorzellen gehen mit der Zeit wieder zugrunde. Es bleiben aber Gedächtnis-B- und Gedächtnis-T-Lymphozyten zurück, welche sich im Falle des Falles sofort an den Krankheitserreger erinnern und diesen abwehren.
Die Immunreaktion auf die Impfung nimmt nach einiger Zeit ab. Die Konzentration der gebildeten schützenden Antikörper nimmt ab. Eine „Booster“-Impfung nach einem bestimmten Zeitintervall (je nach Impfung) stärkt die Abwehr gegen die Krankheitserreger wieder, steigert wieder die Konzentration der Antikörper im Blut (Antikörpertiter) und sorgt für ein besseres/längeres immunologisches Gedächtnis.
Öffnungszeiten
Montag: 14:00 – 19:00
Mittwoch: 10:00 – 14:00
Donnerstag: 14:00 – 19:00
Kontakt
- Alserstraße 48/2, 1090 Wien
- +43 1 4038343
- E-Mail an das Impfzentrum Alserstraße
- Zahlungsarten: Bar, Bankomat und Kreditkarte

